Ministerstvo zdravotnictví poslalo do připomínkového řízení novelu zákona č. 378/2007, o léčivech, která stanovuje pravidla pro ověřování pravosti a neporušenosti balení humánních léčivých přípravků, respektive pro používání ochranných prvků umístěných na jejich obalech. Dokončuje se tak transpozice evropských předpisů, které mají bránit distribuci padělaných léků. Česko již v roce 2013 transponovalo do zákona o léčivech tzv. protipadělkovou směrnici (20011/62/EU), která mj. definuje zmíněné ochranné prvky. Nyní tedy na tuto definici navazují pravidla, jak tyto prvky zavádět a ověřovat, která stanovila Evropská Komise prostřednictvím svého nařízení 2016/161, jímž směrnici doplnila. Připomínkové řízení k zákonu o léčivech je zkráceno na 15 dnů, končí 9. května. Účinnost celé nové protipadělkové legislativy, včetně té části, která byla přijata už v roce 2013, je celoevropsky sladěna na 9. února příštího roku.
Komise zdůvodnila nařízení tím, že má zajistit, „aby systém ověřování léčiv byl využitelný ve všech členských státech Evropské unie, neomezoval oběh léčivých přípravků a nezvyšoval další náklady všech účastníků dodavatelského řetězce způsobené překonáváním národních odlišností“. Nařízení je pro členské státy závazné v celém rozsahu a je ve všech přímo použitelné.
Padělané léky se objevují zejména v nelegálních distribučních kanálech, nabízeny jsou neoprávněnými subjekty na internetu. V legálním dodavatelském řetězci (tj. u povolených distributorů a lékáren) jsou padělky v Evropské unii méně rozšířené, ale riziko jejich vzestupu touto cestou rok od roku roste. Podle důvodové zprávy k novele zákona o léčivech se nejčastěji jedná o léčivé přípravky používané k léčbě sexuální dysfunkce, pálení žáhy, poruch příjmu potravy, úzkosti a onkologických onemocnění. V Česku jsme zatím problém s padělky téměř nezaznamenali, nicméně máme společnou odpovědnost za přijetí opatření, které zabrání jejich šíření v rámci cele EU.
Na obalu humánního léčivého přípravku budou umístěny dva ochranné prvky:

1. Jedinečný identifikátor (unique identifier, UI), který bude mít podobu dvourozměrného (2D) čárového kódu (QR kódu). Je to vlastně série numerických nebo alfanumerických znaků, která je pro dané balení léčivého přípravku jedinečná. Identifikátor se skládá z kódu přípravku (umožňující identifikovat alespoň, běžný název, lékovou formu, sílu, velikost balení a typ balení), sériového čísla, vnitrostátního úhradového čísla, čísla šarže a datumu použitelnosti. Tento ochranný prvek umožňuje ověřit pravost a identifikovat jednotlivé balení léčivého přípravku. Je ke každému balení léku přiřazen v rámci výrobního procesu a bez něj nemůže být toto balení propuštěno na trh.
2. Prostředek k ověření manipulace s obalem (anti-tampering device, ATD), který umožňuje ověřit, zda bylo s obalem léčivého přípravku manipulováno. [mn_protected]
Mohlo by vás zajímat
Nařízení Komise blíže nespecifikuje podobu tohoto prostředku, lze si jej ale představit jako bezpečnostní pojistku proti otevření, která může mít nejrůznější podobu – přelepky, odtrhovací komponenty vnějšího obalu nebo promačkávacího obalu. Pacientovi tato pojistka signalizuje, že on je tím prvním, kdo balení léku otevírá od okamžiku jeho vyrobení. Podle důvodové zprávy je už dnes řada léčivých přípravků tímto bezpečnostním prvkem vybavena na dobrovolné bázi.
Ucelený ověřovací systém vyžaduje zřízení systému úložišť, ve kterých budou mimo jiné obsaženy informace o jedinečných identifikátorech jednotlivých balení léčivých přípravků.
Systém úložišť zřídí a spravují neziskové právní subjekty, skládá se z centrálního úložiště a úložiště, která slouží území jednoho členského státu („vnitrostátní úložiště“), nebo územím více členských států („nadnárodní úložiště“), která musí být připojena k centrálnímu úložišti.
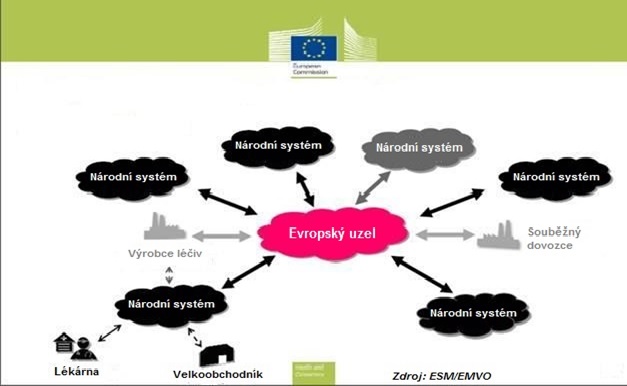
Evropská organizace pro ověřování léčiv (European Medicines Verification Organisation, EMVO) představuje neziskovou organizaci založenou evropskými asociacemi či sdruženími zejména z řad farmaceutického průmyslu, farmaceutických společností, distributorů a lékárníků. Hlavním úkolem této organizace je zřízení a správa centrálního úložiště (European Hub). V České republice byla jako neziskový právní subjekt založena Národní organizace pro ověřování pravosti léčiv, z. s. (NOOL), jejímiž členy jsou Asociace inovativního farmaceutického průmyslu (AIFP), Česká asociace farmaceutických firem (ČAFF), Asociace evropských distributorů léčiv (AEDL), Asociace velkodistributorů léčiv – AVEL, z.s., Česká lékárnická komora.
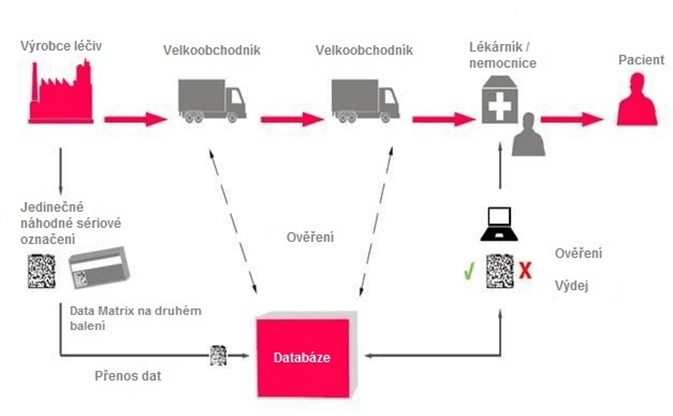
Výrobci budou mít povinnost opatřit balení předmětných léčivých přípravků ochrannými prvky a ověřit, že jedinečný identifikátor je čitelný a obsahuje informace dané nařízením o ochranných prvcích. Držitelé rozhodnutí o registraci nebo odpovědná osoba v případě souběžně dovážených nebo distribuovaných léčivých přípravků musí zajistit, aby informace o jedinečných identifikátorech byly do systému úložišť nahrány před tím, než bude léčivý přípravek uveden na trh.
Distributoři budou ověření ochranných prvků provádět jen v případě léčivých přípravků, u kterých existuje vyšší riziko padělání (tj. u léčivých přípravků vrácených osobami oprávněnými vydávat léčivé přípravky nebo jiným distributorem).
Lékárníci před výdejem pacientovi ověří oba ochranné prvky a provedou vyřazení jedinečného identifikátoru ze systému úložišť v okamžiku výdeje pacientovi. Při ověření se porovná identifikátor na obalu s identifikátorem v úložišti. Ověření neporušenosti prostředku k ověření manipulace s obalem bude se provede vizuální kontrolou.
Do zákona o léčivech se nařízení promítlo v několika dalších bodech:
- Určuje se vnitrostátní orgán, který bude mít přístup k úložišti pro účely dozoru nad jeho fungováním, vyšetřování potenciálních případů padělání, úhrady, farmakovigilance a farmakoepidemiologie. Tímto orgánem bude Státní ústav pro kontrolu léčiv (SÚKL).
- Vymezují se skutkové podstaty přestupků v této oblasti, určením správního orgánu příslušného k jejich projednávání a stanovením výše sankcí za neplnění povinností regulovanými subjekty. Sankce zohledňují ohrožení veřejného zdraví, které představuje padělání léčivých přípravků, stanovena je jejich horní hranice, jednotlivé prohřešky jsou oceněny částkami 2, 5 a 20 miliónů korun.
- Česko nebude rozšiřovat oblast působnosti ochranných prvků na některé další léčivé přípravky, i když to EU členským státům umožňuje.
- Nařízení uvádí pojem „vnitrostátní úhradové číslo“, tím bude v česku dosavadní kód SÚKL, který tak na obalech léků zůstává.
- Členský stát má zohlednit zvláštní charakteristiky dodavatelského řetězce na svém území a umožnit ve své právní úpravě, aby distributor ověřil ochranné prvky a provedl vyřazení jedinečného identifikátoru léčivého přípravku před tím, než léčivý přípravek vydá některé z osob nebo institucí. V CR budou těmito institucemi pouze veterinární lékaři a armáda.
- V polovině roku 2009 došlo v ČR ke změně distribuce imunologických přípravků (ne již přes krajské hygienické stanice, ale přes distribuční firmu). Aby bylo možno zachovat tento systém dodávek přímo do ordinací poskytovatelů zdravotních služeb, a nebylo ohroženo očkování dětí a dospělých, je přenesena povinnost vyplývající z nařízení o ochranných prvcích na distributora imunologických přípravků. Distributor jako osoba zmocněná k výdeji léčivých přípravků, a to pouze v případě dodávek imunologických přípravků přímo do ordinací lékařů za účelem očkování, provede ověření ochranných prvků a vyřazení jedinečného identifikátoru ze systému úložišť před tím, než dodá imunologické přípravky poskytovatelům zdravotních služeb za účelem očkování.
[/mn_protected]
-cik-